方信賢1, 2,  , 薛亞軍1, 戴玉明1, 王章忠1, 2
, 薛亞軍1, 戴玉明1, 王章忠1, 2
1 南京工程學院江蘇省先進結構材料與應用技術重點實驗室, 南京 211167
2 南京工程學院材料工程學院, 南京 211167
摘要
分別采用浸泡和電化學實驗方法對Ni-W-Cu-P鍍層在常溫和高溫20%H2SO4溶液中的耐蝕性進行了研究, 用SEM, EDS及XRD對鍍層的沉積機制、成分結構進行了分析. 結果表明: 球形Ni-W-Cu-P核心合并生長形成條狀組織; 共沉積W和Cu可顯著提高Ni-W-Cu-P非晶的熱穩定性; 400 ℃熱處理非晶的耐蝕性優于鍍態非晶和500 ℃熱處理納米晶的; 延長腐蝕時間, 非晶和納米晶鍍層的腐蝕速率和腐蝕電流密度增大, 阻抗則下降; Ni-W-Cu-P非晶和納米晶鍍層的腐蝕機制分別是選擇性腐蝕和點腐蝕.
關鍵詞: Ni-W-Cu-P鍍層, ; 沉積機制, ; 酸性腐蝕介質, ; 腐蝕機制, ; 阻抗譜
酸性腐蝕環境是工程中金屬構件常見的服役環境之一, 該環境中因Fe具有較高化學活性, 致使鋼鐵構件在該類環境中的工程應用因耐蝕性不足而面臨嚴峻挑戰, 表面改性是解決該問題的有效途徑之一. 研究[1,2]表明, 化學鍍Ni-P鍍層具有優異的抗靜態腐蝕和沖刷腐蝕性能, 尤其是在溫度較高的酸性環境, 其耐蝕性顯著優于該類環境常用材料316L不銹鋼. 合金元素W和Cu常被用于進一步改善Ni-P合金鍍層性能, 據報道, 三元Ni-W-P合金鍍層在NaCl溶液[3,4]和H2SO4溶液[5,6]中的抗腐蝕性能優于Ni-P合金鍍層; W具有較高的硬度, 而在熱處理時會形成Ni-W固溶體[7], 使Ni-W-P合金鍍層具有較Ni-P合金鍍層更高的硬度[7,8]及耐磨性能[9,10]; W還賦予Ni-W-P合金鍍層較Ni-P合金鍍層更好的熱穩定性[7,11]. 而在Ni-P鍍層中共沉積Cu制備的三元Ni-Cu-P合金鍍層, 其在H2SO4溶液中具有較Ni-P鍍層更優異的靜態腐蝕和沖刷腐蝕性能[12,13]; 在60 ℃的高溫燃氣冷凝水中, Ni-Cu-P的耐蝕性明顯優于Ni-P合金鍍層[14]. 在Ni-P合金鍍層中同時共沉積W和Cu制備四元Ni-W-Cu-P合金鍍層的研究報道較少, 據Balaraju和Rajam[15]報道, 在Ni-W-P鍍液中添加CuSO4可制得表面較Ni-W-P鍍層更平坦的Ni-W-Cu-P鍍層, 且Ni-W-Cu-P鍍層不僅在3.5%NaCl (質量分數)溶液和1 mol/L HCl溶液中的耐蝕性優于Ni-W-P鍍層, 而且在Ni-W-P鍍層中共沉積Cu對鍍層的硬度影響較小.
目前, 有關化學鍍四元Ni-W-Cu-P合金鍍層沉積機制、腐蝕介質溫度及腐蝕時間對其耐蝕性及腐蝕機制的影響等鮮見報道. 為此, 本工作在對化學鍍Ni-P和Ni-Cu-P鍍層研究的基礎上, 以65Mn為基體, 通過在化學鍍Ni-Cu-P鍍液中添加Na2WO4, 制備了Ni-W-Cu-P四元合金鍍層, 并就上述問題進行了系統研究.
1 實驗方法
化學鍍Ni-W-Cu-P基體試樣為65Mn冷軋圓片試樣, 試樣直徑為25.4 mm, 厚為2.0 mm. 化學鍍液采用HHS-1恒溫水浴鍋加熱保溫, 鍍液溫度為(83±1) ℃. 基體試樣經過堿性除油、水洗、酸洗和水洗后, 吊掛在自行研制的高溫堿性Ni-W-Cu-P化學鍍液中分別化學鍍1, 5, 10, 20, 30, 60和120 min, 得到分析Ni-W-Cu-P鍍層沉積機制的試樣. 將化學鍍120 min的部分試樣分別放入已升溫到400和500 ℃的箱式電阻爐中保溫2 h, 得到不同溫度熱處理的Ni-W-Cu-P試樣.
用浸泡腐蝕實驗法評定常溫(20 ℃)下鍍態和熱處理態Ni-W-Cu-P鍍層在濃度為20%H2SO4 (體積分數)溶液中的耐蝕性, 用FA1004分析電子天平測量試樣腐蝕前后的質量, 根據公式v0=Δm/(St)計算靜態腐蝕速率(式中, v0為腐蝕速率, Δm為腐蝕前后試樣的質量差, S為試樣的表面積, t為浸泡腐蝕時間).
用電化學方法評定鍍態和熱處理態Ni-W-Cu-P鍍層在50 ℃, 20%H2SO4溶液中的高溫耐蝕性, 用PARSTAT2273電化學工作站檢測Ni-W-Cu-P鍍層的極化曲線和交流阻抗譜(EIS), 介質溫度用HHS-1恒溫水浴控制. 采用標準三電極系統, 參比電極為飽和甘汞電極(SCE), 輔助電極為Pt電極, 工作電極為樣品; 用樣品做工作電極時, 留出的工作面尺寸為10 mm×10 mm, 其它表面用環氧樹脂封固; 極化曲線測試動電位掃描速率為2 mV/s, 根據強極化區外加電流與電極極化的關系, 用Tafel直線外推法計算得到自腐蝕電流密度icorr; EIS測試采用開路電位測量, 頻率范圍為100 mHz~100 kHz, 以Bode圖中低頻阻抗模值評定鍍層耐蝕性.
用JSM6360LVX型掃描電鏡(SEM)觀察腐蝕前后鍍層的表面形貌, 用GENESIS2000XMS60型能譜儀(EDS)分析化學成分. 用UltmaⅣ型X射線衍射儀(XRD)對Ni-W-Cu-P鍍層的結構進行分析.
2 實驗結果與分析
2.1 化學鍍時間對Ni-W-Cu-P組織及成分影響
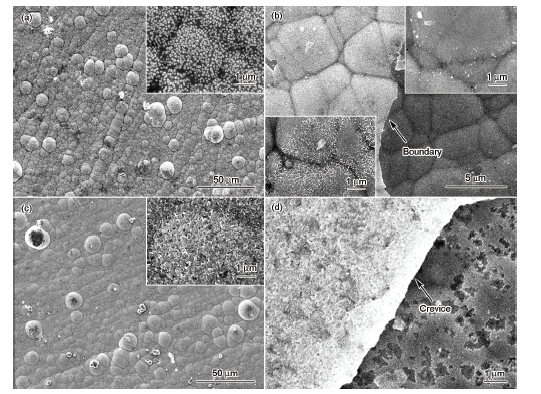
圖1為化學鍍不同時間Ni-W-Cu-P鍍層的表面形貌. 可見, 化學鍍1 min時(圖1a), 在試樣表面形成了灰色多孔鍍層, 在灰色多孔鍍層表面均勻分布著少量尺寸較大的白色塊狀顆粒和許多尺寸較小的白色納米顆粒, 在灰色鍍層中還可見許多尺寸與白色納米顆粒相近的黑色孔洞, 這些黑色納米孔洞與化學鍍初期宏觀觀察到試樣表面大量氫氣釋放在界面區內形成劇烈的攪拌, 導致試樣表面形成的部分核心剝落有關. 對白色顆粒A和B, 灰色平坦區C和黑色孔洞D進行EDS分析(表1), 結果可見, 其Ni, W, Cu和P的質量分數存在明顯差異, 表明化學鍍初期形成的鍍層成分分布存在明顯的微觀不均勻性. 化學鍍5 min時(圖1b), 試樣表面均勻分布著以亞微米尺寸為主的球形顆粒, 同時還可見少量球形顆粒合并生長形成的尺寸較大的白亮顆粒(如圖1b中箭頭E所示), 對圖1b中箭頭F所示白亮顆粒和箭頭G所示鄰近尺寸較小的灰色顆粒的EDS分析(表1)表明, 此時形成的鍍層中不同顆粒其W和P的質量分數仍存在較大的差異. 化學鍍10 min時(圖1c), Ni-W-Cu-P球形顆粒平均尺寸明顯增大, 同時鍍層表面開始出現球形顆粒合并生長形成的尺寸較大的條狀組織(如圖1c箭頭H所示), 經EDS分析(表1), 與箭頭I所示鄰近球形小顆粒相比, Cu的質量分數相近, 而W和P的質量分數差別較大, 與化學鍍5 min同類型的組織成分相比, 非合并生長的小顆粒成分相近, 而合并生長的大顆粒, Cu和W的質量分數相近, 但P的質量分數明顯提高. 化學鍍20 min時(圖1d), 試樣表面形成了由球形顆粒合并生長形成的條形組織, 化學鍍30 min (圖1e)形成的條形組織與化學鍍20 min時的類似, 較長時間化學鍍后, 條形組織中的胞狀顆粒尺寸明顯增大(圖1f). 由上述分析可見, 化學鍍初期形成的Ni-W-Cu-P核心有球形和塊狀2種, 化學鍍大約5 min后, 隨著試樣表面與鍍液間較穩定界面區的建立, 此時形成的Ni-W-Cu-P核心均為球形核心, 而球形核心的合并生長導致條狀Ni-W-Cu-P組織的形成.
圖1 化學鍍不同時間Ni-W-Cu-P鍍層的SEM像
Fig.1 SEM images of Ni-W-Cu-P coatings after plating for different times(a) 1 min (b) 5 min (c) 10 min (d) 20 min (e) 30 min (f) 120 min
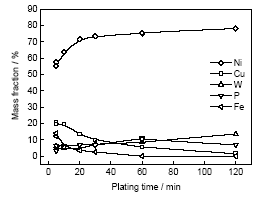
圖2為Ni-W-Cu-P鍍層化學成分隨化學鍍時間(t)的變化曲線. 可見, 化學鍍5 min后, 隨化學鍍時間延長, 鍍層中Ni的質量分數按對數規律增大(wNi=7.12lnt+46.61), Cu的質量分數按對數規律減小(wCu=-6.18lnt+31.18), W的質量分數按線性規律增大(wW=0.073t+4.45), P的質量分數按拋物線規律變化(wP=-0.0013t2+0.18t+4.03), 在5~60 min內, Fe的質量分數按對數規律急劇下降(wFe=-5.10lnt+20.07), 在化學鍍60 min后形成的鍍層中沒有檢測到元素Fe. 鍍層中合金元素質量分數隨化學鍍時間延長發生變化, 與化學鍍期間隨著氫氣釋放, 鍍液與試樣表面間形成的界面區內pH值發生變化有關[16,17].
圖2 Ni-W-Cu-P鍍層成分隨化學鍍時間的變化
Fig.2 Variation of chemical composition of Ni-W-Cu-P coatings with plating time
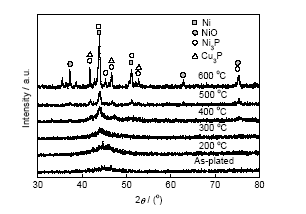
圖3為不同溫度保溫2 h的Ni-W-Cu-P鍍層的XRD譜. 可見, 鍍態和400 ℃以下熱處理的Ni-W-Cu-P鍍層的XRD譜為漫散的饅頭峰, 說明這些鍍層具有非晶結構, 當熱處理溫度達到500 ℃及以上時, 鍍層的XRD譜出現較尖銳的衍射峰, 表明此時鍍層已由非晶轉變為混晶或晶態結構, 根據Ni(W)固溶體(111)衍射峰, 用Scherrer法計算表明, Ni(W)固溶體的晶粒尺寸為41.5 nm, 因此, 500 ℃熱處理的鍍層為納米晶鍍層. 據報道, Ni-Cu-P[18,19]和Ni-W-P[10,20]合金鍍層在400 ℃熱處理時均發生了明顯晶化, 表明在Ni-P合金中同時共沉積W和Cu制備的四元Ni-W-Cu-P非晶合金較單獨共沉積W或Cu制備的三元Ni-W-P或Ni-Cu-P非晶合金具有更好的熱穩定性.
圖3 不同溫度熱處理后Ni-W-Cu-P鍍層的XRD譜
Fig.3 XRD spectra of Ni-W-Cu-P coatings annealed at different temperatures
2.2 Ni-W-Cu-P常溫耐蝕性及腐蝕機制
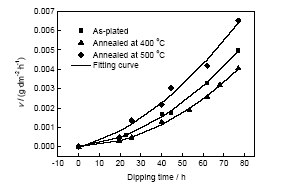
圖4為不同溫度熱處理的Ni-W-Cu-P鍍層在常溫20%H2SO4溶液中浸泡腐蝕不同時間(td)后測量的腐蝕速率(v)及用二次多項式v= (其中, a, b, c為擬合常數)擬合的匹配曲線. 由圖4可見, Ni-W-Cu-P鍍層的腐蝕速率隨著浸泡腐蝕時間延長按拋物線規律增大. 在腐蝕時間相同時, Ni-W-Cu-P鍍層的腐蝕速率由大到小依次為500 ℃熱處理納米晶鍍層、鍍態非晶鍍層和400 ℃熱處理的非晶鍍層, 表明400 ℃熱處理非晶鍍層具有較鍍態非晶和500 ℃熱處理納米晶鍍層更好的抗腐蝕性能.
圖4 不同溫度熱處理Ni-W-Cu-P鍍層的腐蝕速率隨浸泡時間變化曲線
Fig.4 Variation of corrosion rate (v) of Ni-W-Cu-P coatings annealed at different temperatures with dipping time
圖5為Ni-W-Cu-P鍍層常溫腐蝕不同時間后的表面形貌. 由圖5a可見, 鍍態非晶鍍層腐蝕19.5 h后, 低倍下仍為典型胞狀結構, 但高倍下腐蝕表面均勻分布尺寸約100 nm的納米顆粒(圖5a插圖). 因為球形顆粒合并生長形成的胞狀組織中顆粒界面能高于顆粒內部的, 導致沿顆粒界面的腐蝕速率大于顆粒內部的, 故球形顆粒腐蝕殘留物納米顆粒在胞狀組織表面的分布也非常均勻. EDS分析(表2)表明, 納米顆粒(NP)中Ni含量略高于納米顆粒間基體(M)的, 而Cu和W含量則相反, 這種成分差異是因為Cu的電極電位高于Ni的, 使Ni優先Cu腐蝕[14], 導致腐蝕較深的納米顆粒間鍍層與納米顆粒產生成分差異. 上述分析表明, 鍍態Ni-W-Cu-P鍍層在常溫H2SO4溶液中發生的是選擇性腐蝕.
圖5 Ni-W-Cu-P鍍層腐蝕不同時間后的表面形貌
Fig.5 Surface morphologies of Ni-W-Cu-P coatings after corroded for different times (Insets show high magnified images) (a) as-plated, 19.5 h (b) annealed at 400 ℃, 25.5 h (c) annealed at 500 ℃, 19.5 h (d) annealed at 500 ℃, 44.5 h
400 ℃熱處理的Ni-W-Cu-P鍍層腐蝕25.5 h后, 低倍下腐蝕表面由白亮和灰色胞狀組織組成(圖5b), 在2種組織交界處可見, 包覆在灰色胞狀組織表面的“蛋殼狀”白亮膜邊緣輪廓清晰, 且與被包覆的灰色胞狀組織間沒有明顯縫隙, 表明它們間的界面結合良好. EDS分析見表2, 白亮胞狀組織(WCS)中存在較高含量O, 而灰色胞狀組織(GCS)中不含O, 表明白亮膜是尚未溶解掉的氧化膜; 此外, 氧化膜和灰色胞狀組織在鍍層縱向所處位置相近, 其Ni, W和Cu含量應相近, 但灰色胞狀組織中的Ni含量明顯低于氧化膜中的, 而W和Cu含量則正好相反, 表明400 ℃熱處理的Ni-W-Cu-P非晶鍍層在常溫H2SO4溶液中也發生了Ni優先溶解現象, 故其腐蝕機制也是選擇性腐蝕. 高倍觀察顯示, 灰色胞狀組織表面形貌與鍍態非晶腐蝕后的不同, 其表面沒有均勻分布的納米顆粒(圖5b右上角插圖), 表明非晶胞狀組織中原球形顆粒合并生長形成的低能界面在400 ℃熱處理時已經消失. 對氧化膜高倍觀察發現, 該膜為片狀氧化物圍成的網絡狀多孔結構(圖5b左下角插圖), 因片狀氧化物嵌入非晶鍍層基體內形成嵌入式結構, 使400 ℃熱處理形成的氧化膜與非晶鍍層基體間具有較高的界面結合力.
由圖5c可見, 500 ℃熱處理的Ni-W-Cu-P納米晶鍍層腐蝕19.5 h后, 低倍下其表面仍為典型胞狀結構, 高倍下則為多孔結構(圖5c插圖), EDS分析(表2)顯示, 胞狀組織(CS)中含較多的O, 表明此時其表面仍被多孔氧化膜包覆. 腐蝕44.5 h后, 鍍層表面由白亮區和灰色區組成(圖5d), EDS分析(表2)表明, 白亮區組織(WS)為尚未溶解掉的氧化膜, 灰色區組織(GS)為氧化膜溶解后裸露的納米晶鍍層. 在白亮氧化膜與灰色納米晶交界處可見, 氧化膜與其包覆的納米晶鍍層間存在明顯縫隙, 表明500 ℃熱處理時形成的氧化膜與納米晶鍍層間結合力較差. 在裸露出的納米晶表面存在許多納米尺度孔洞, 結合圖3 XRD分析結果可見, 這些納米孔洞是由于500 ℃熱處理時形成的納米級磷化物顆粒(如Ni3P)溶解或剝落后, 孔內壁進一步腐蝕形成的. 綜上可知, Ni-W-Cu-P納米晶鍍層的腐蝕機制是點腐蝕.
根據腐蝕后鍍層表面形貌觀察可見, 與400 ℃熱處理非晶相比, 一方面, 鍍態非晶腐蝕后表面形成了大量納米顆粒, 增大了其表面與腐蝕介質間的接觸面積, 另一方面, 胞狀組織中球形顆粒間界面能相對較高, 導致鍍態非晶的耐蝕性低于400 ℃熱處理非晶的. 與非晶鍍層相比, 500 ℃熱處理的納米晶不僅具有晶界、相界等高能缺陷, 而且, 熱處理時形成的氧化膜與內部納米晶鍍層間結合力較差, 當氧化膜發生局部溶解破損后, 進入縫隙的腐蝕液將使氧化膜面臨雙向腐蝕, 同時, 氧化膜溶解破損后裸露的納米晶鍍層與腐蝕液的接觸面積也將增大, 從而導致納米晶鍍層的耐蝕性不如非晶的.
2.3 Ni-W-Cu-P高溫耐蝕性及機制
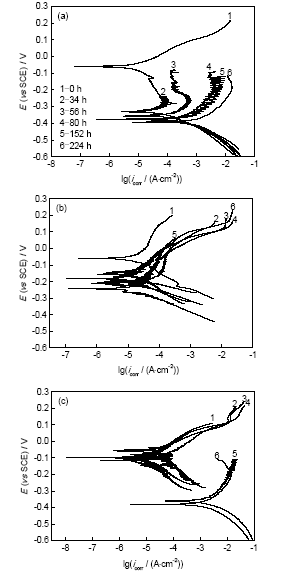
圖6為Ni-W-Cu-P鍍層的動電位極化曲線, 腐蝕不同時間后鍍層的腐蝕電流密度如表3所示. 由圖6a可見, 鍍態非晶鍍層腐蝕34 h后, 腐蝕電位顯著負移(262 mV), 進一步延長腐蝕時間, 腐蝕電位單調負移值較小; 由表3可見, 鍍層的腐蝕電流密度隨腐蝕時間延長單調增大, 腐蝕56 h后腐蝕電流密度顯著增大. 由圖6b可見, 400 ℃熱處理的非晶鍍層, 腐蝕時間低于152 h時, 腐蝕電位隨腐蝕時間延長單調負移, 但在腐蝕224 h后, 腐蝕電位發生了小幅正移; 與鍍態非晶鍍層相比, 該鍍層在長期腐蝕期間, 雖然腐蝕電流密度隨腐蝕時間延長呈單調增大趨勢, 但其腐蝕電流密度增大幅度較小, 其腐蝕224 h后的腐蝕電流密度僅約為未腐蝕鍍層的1.9倍, 而鍍態非晶鍍層腐蝕224 h后的腐蝕電流密度則約為未腐蝕鍍層的526倍, 這說明400 ℃熱處理非晶鍍層在高溫H2SO4溶液中具有較鍍態非晶鍍層更好的抗長期腐蝕性能. 由圖6c可見, 500 ℃熱處理的納米晶鍍層在腐蝕時間低于80 h時, 其腐蝕電位接近, 腐蝕電流密度隨腐蝕時間延長略有增大; 腐蝕152 h后, 其腐蝕電位明顯負移, 腐蝕電流密度則顯著增大. 與400 ℃熱處理非晶鍍層相比, 當腐蝕時間小于80 h時, 其腐蝕電流密度與400 ℃熱處理非晶鍍層的接近, 進一步延長腐蝕時間, 2種鍍層間的腐蝕電流密度差異顯著增大(表3), 在腐蝕224 h時, 納米晶鍍層的腐蝕電流密度為400 ℃熱處理非晶鍍層的479.3倍, 表明500 ℃熱處理的納米晶鍍層在高溫H2SO4溶液中具有較差的抗長期腐蝕性能.
圖6 不同溫度熱處理的Ni-W-Cu-P鍍層極化曲線
Fig.6 Polarization curves of Ni-W-Cu-P coatings as-plated (a), annealed at 400 ℃ (b) and at 500 ℃ (c) (E—potential, icorr—current density)
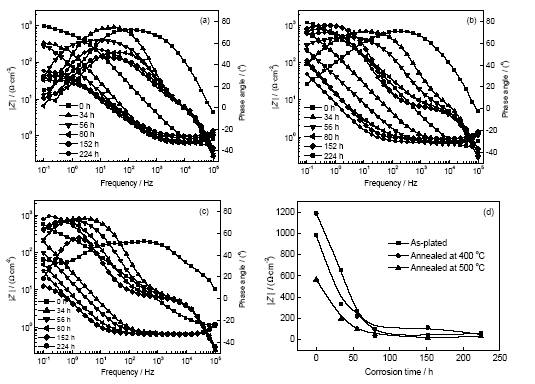
圖7為Ni-W-Cu-P鍍層的Bode圖及其阻抗隨腐蝕時間變化曲線. 由圖7可見, 在中低頻區, 鍍態和熱處理態鍍層的阻抗均隨著腐蝕時間延長而減小, 當腐蝕時間小于80 h時, 鍍層的阻抗隨腐蝕時間延長快速下降, 進一步延長腐蝕時間, 鍍層的阻抗變化較小. 根據阻抗的大小可見, 400 ℃熱處理的非晶鍍層耐蝕性最好, 鍍態非晶鍍層耐蝕性居中, 500 ℃熱處理的納米晶鍍層耐蝕性最差, 該實驗結果與極化曲線分析結果一致. 此外, 鍍層最大相位角接近90°, 說明鍍層表現為電容性質, 隨著腐蝕時間延長, 最大相位角向低頻方向移動, 表明隨著腐蝕時間延長, 鍍層表面膜層發生了變化[21].
圖7 Ni-W-Cu-P鍍層的Bode圖及其阻抗隨腐蝕時間的變化曲線
Fig.7 Bode plots for as-plated Ni-W-Cu-P coatings (a), and then annealed at 400 ℃ (b) and 500 ℃ (c), and variation of their impedance values (|Z|) with corrosion time (d)
由表3和圖7還可見, 當腐蝕時間較短時, 鍍層的阻抗變化較明顯, 因而此時用阻抗表征鍍層的耐蝕性好壞具有更高的靈敏度, 而當腐蝕時間較長時, 腐蝕電流密度的變化較明顯, 因而此時腐蝕電流密度能更靈敏地反映鍍層耐蝕性的優劣.
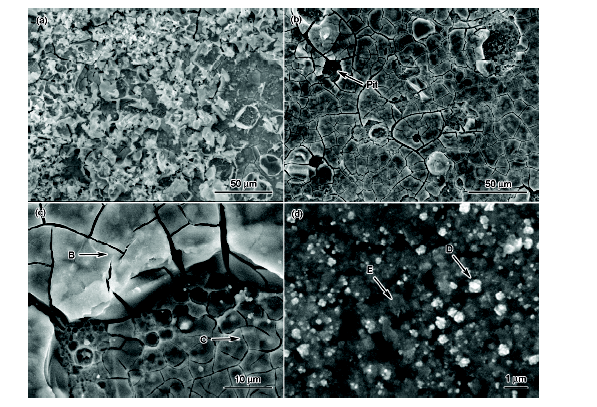
圖8為Ni-W-Cu-P鍍層高溫腐蝕224 h后的表面形貌像. 由圖8a可見, 鍍態非晶表面形成了非連續的腐蝕產物膜, EDS分析(表4, A)表明, 該膜層中Ni元素質量分數低于鍍層中Ni的最低質量分數, 而W和P的質量分數則高于鍍層中最大質量分數的(圖2), 表明鍍態非晶在高溫H2SO4溶液中發生了較嚴重的選擇性腐蝕. 由圖8b可見, 400 ℃熱處理非晶腐蝕224 h后, 表面形成了類似干枯河床“干泥巴狀”連續腐蝕產物膜, 局部位置可見腐蝕產物膜脫落后形成的凹坑, 高倍觀察表明, 腐蝕產物膜的厚度在5 μm左右, 而腐蝕產物膜脫落位置形成了新的腐蝕產物膜(圖8c), EDS分析(表4)表明, 箭頭所示未脫落位置B腐蝕產物膜和脫落位置C新形成的腐蝕產物膜的元素組成和含量存在明顯差異, 表明400 ℃熱處理非晶鍍層發生了較嚴重的選擇性腐蝕. 由于與腐蝕介質接觸的表面由起始時的氧化膜逐漸過渡到由氧化物(如WO3)、硫酸鹽等組成的連續鈍化膜, 導致其腐蝕不同時間后測量的最大相位角由中頻向低頻變化. 此外, 在試樣表面形成的連續鈍化膜中W含量高達24.63%, 而WO3在H2SO4溶液中具有熱力學穩定性[6], 因而表面形成的該鈍化膜對內部鍍層具有較好的保護作用, 這與該鍍層經歷較長時間浸泡腐蝕后仍具有較低的腐蝕電流密度的實驗結果一致. 由圖8d可見, 500 ℃熱處理的納米晶鍍層腐蝕224 h后, 表面較均勻分布著白色納米顆粒和納米孔洞, EDS分析(表4)表明, 箭頭所示白色顆粒D中Ni含量明顯高于灰色基體E中的, 表明白色顆粒是500 ℃熱處理后在鍍層中形成的納米Ni3P顆粒, 灰色基體中W含量明顯高于白色顆粒中的, 表明灰色基體是Ni(W)固溶體. 由于磷化物與固溶體間存在較高的相界面能, 而磷化物與Ni(W)固溶體間因電極電位不同又易引起原電池腐蝕[22], 導致納米磷化物顆粒與Ni(W)固溶體間因腐蝕而脫開剝落, 從而在試樣表面形成了這些均勻分布的納米孔洞. 綜上可見, 納米晶鍍層在高溫H2SO4溶液中發生的是點腐蝕, 與非晶鍍層相比, 納米晶鍍層經過一定時間腐蝕后其表面沒有形成具有一定防護作用的鈍化膜, 導致其長期腐蝕時耐蝕性不如非晶的.
圖8 Ni-W-Cu-P鍍層腐蝕224 h后的SEM像
Fig.8 SEM images of Ni-W-Cu-P coatings after corroding for 224 h (a) as-plated (b, c) annealed at 400 ℃ (d) annealed at 500 ℃
3 結論
(1) 化學鍍初期形成的Ni-W-Cu-P核心有球形和塊狀2種形貌, 化學鍍5 min后均形成球形核心, 球形核心合并生長形成條狀組織.
(2) 隨化學鍍時間延長, 鍍層中Ni, Cu, W, P和Fe的質量分數分別具有對數增大, 對數減小, 線性增大, 拋物線和對數減小變化趨勢.
(3) 在常溫和高溫H2SO4溶液中, Ni-W-Cu-P鍍層耐蝕性由高到低依次為: 400 ℃熱處理非晶、鍍態非晶和500 ℃熱處理納米晶; 常溫下鍍層的腐蝕速率隨腐蝕時間延長按拋物線關系增大, 高溫下鍍層的腐蝕電流密度隨腐蝕時間延長而增大, 阻抗則減小.
(4) 在常溫和高溫H2SO4溶液中, Ni-W-Cu-P非晶和納米晶鍍層的腐蝕機制分別為選擇性腐蝕和點腐蝕.
 , 薛亞軍
, 薛亞軍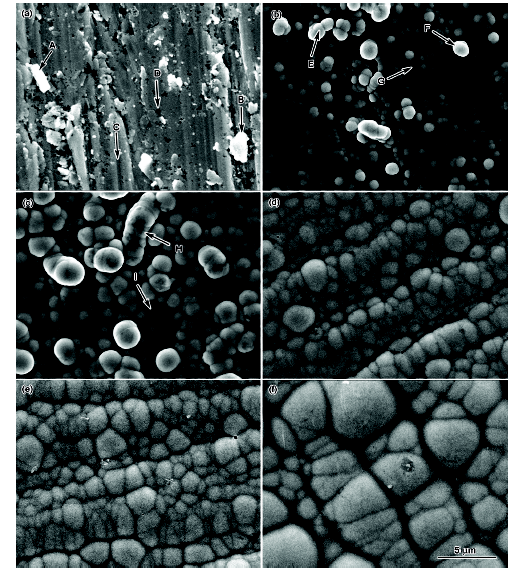






 滬公網安備31011202020290號
滬公網安備31011202020290號
